Paracetamol

DATOS QUÍMICOS
- Nombre sistematico: N-(4-hidroxifenil)etanamida.
- Nombre tradicional: N-acetil-para-aminofenol
- Formula condensada: C8H9NO2,
- Peso mol: 151.17 g/mol
DATOS FÍSICOS
- Densidad: 1,263 g/cm³
- Punto de fusion: 169 °C
- Solubilidad en agua: 12,78 mg/mL a los 20ºC
DEFINICIÓN Y UTILIDADES
El paracetamol o acetaminofén es un fármaco con propiedades analgésicas, sin propiedades antiinflamatorias clínicamente significativas. Actúa inhibiendo la síntesis de prostaglandinas, mediadores celulares responsables de la aparición del dolor. Además, tiene efectos antipiréticos. Se presenta habitualmente en forma de cápsulas, comprimidos, supositorios o gotas de administración oral.
Es un ingrediente frecuente de una serie de productos contra el resfriado común y la gripe. A dosis estándar es casi seguro, pero su bajo precio y amplia disponibilidad han dado como resultado frecuentes casos de sobredosificación. En las dosis indicadas el paracetamol no afecta a la mucosa gástrica ni a la coagulación sanguínea o los riñones, pero sí al hígado, severamente.
A diferencia de los analgésicos opioides, no provoca euforia ni altera el estado de humor del paciente. Al igual que los antiinflamatorios no esteroideos, no se asocia con problemas de adicción, tolerancia y síndrome de abstinencia.
SÍNTESIS
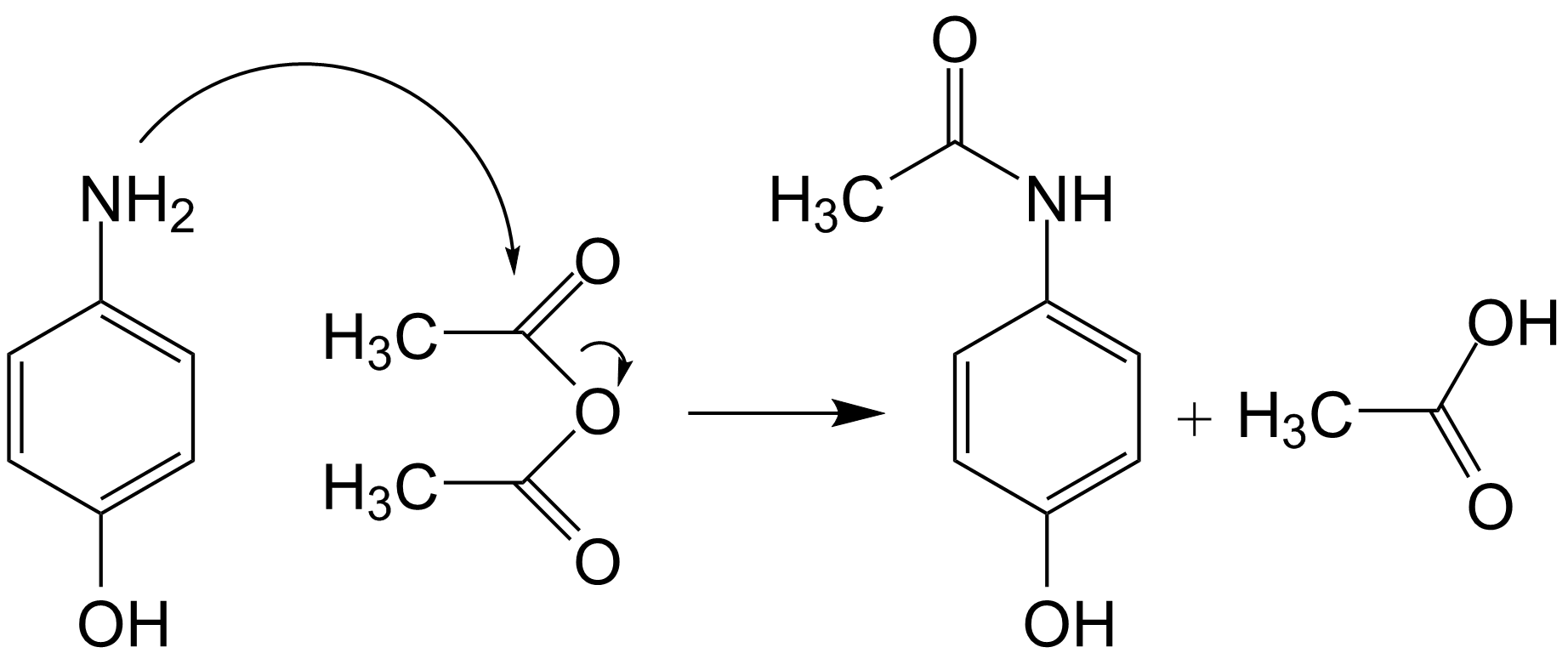
Las reacción del p-aminofenol con anhídrido acético, produce la acetilación del primero, obteniéndose como productos el paracetamol y ácido acético.
TOXICIDAD
El paracetamol no debe tomarse tras consumir alcohol, debido a que el hígado, cuando está metabolizando el alcohol, no puede metabolizar simultáneamente el paracetamol, aumentando por tanto el riesgo de hepatotoxicidad
no tiene efectos negativos sobre el esófago, estómago, intestino delgado o intestino grueso. El ayuno es un factor de riesgo, posiblemente debido a la reducción de las reservas de glutatión del hígado.