Ciclo de Born-Haber
El ciclo de Born-Haber es un ciclo termodinámico en el que se estudian todos los procesos que intervienen en la formación de un mol de un compuesto iónico a partir de los elementos que lo integran, estos se encuentran en su estado termodinámico más estable.
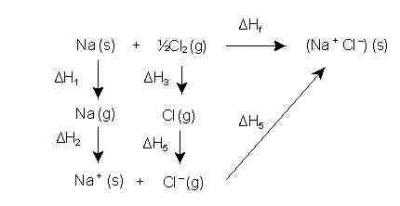
El proceso de formación del cloruro de sodio (sólido), a partir de sodio (sólido) e de cloro (gas), podemos considerarlo como la suma de los siguientes procesos:
1. Sublimación del sodio sólido en sodio gas (se utiliza la energía de sublimación). Na(s) a Na(g).
2. Ionización del Na (g) a Na+ (interviene la energía de ionización).
3. Disociación de las moléculas de cloro (Cl2), en átomos de cloro separados (se utiliza la energía de enlace).
4. Ionización del Cl (g) a Cl- (g) (interviene la afinidad electrónica).
5. En el último paso interviene la energía de red(energía que se desprende al formar un mol de cristal iónico sólido a partir de sus correspondientes iones en estado gaseoso).
Una forma de analizar la estabilidad de la red cristalina iónica es interpretando las etapas teóricas que permiten llegar desde los elementos hasta el cristal iónico.
Si se toma el ejemplo de la formación del NaCl:
Como se observa en el esquema, se puede llegar a formar NaCl(s) por dos caminos diferentes. .
Aplicando la Ley de Hess, se puede deducir que:
ΔHf=ΔH1+ΔH2+ΔH3+ΔH4+ΔH5 siendo ΔH5 la energía reticular o de red (U)
Según la Ley de Hess, la entalpía intercambiada en una reacción es la misma, tanto si el proceso se realiza en una sola etapa, como si tiene lugar en varias.
0 comentarios