Estructura de Lewis y Geometría del ácido sulfúrico
Para realizar la estructura de Lewis, en primer lugar...
Designamos el átomo central, el azufre (el menos electronegativo, de la molécula), y colocamos alrededor de él los átomos de oxígeno. A dos de estos (oxígenos) se le enlazan los hidrógenos.
Calculamos el numero total de electrones de valencia. (nt)
Calculamos el número total de electrones enlazados, en la molécula. (nee)
Obtenemos el número de electrones sin enlazar (libres). (nese)
Los pares no enlazantes deben colocarse alrededor de cada átomo de modo que todos adquieran estructuras de gas noble (mayor estabilidad)
En segundo lugar...
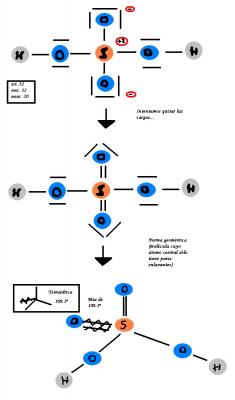
Quitamos las cargas formales, colocando dobles o triples enlaces (en este caso enlaces dobles) para que queden con carga neutra. Colocamos dos dobles enlaces para neutralizar la carga (-) de los dos Oxígenos (O) captando esa carga el Azufre que tiene como carga (+2).
En tercer lugar, realizamos la geometría del H2SO4 ...
Al ser una molécula cuyo átomo central sólo tiene pares enlazantes, la repulsión entre ellos hace que éstos se dispongan en una geometría tetraédrica, con ángulos de 109.5 º aproximadamente.
2 comentarios
KarenPat -
CON ESA ESTRUCTURA DESPEJÉ MI DUDA, YA QUE AL HACERLA LINEAL RESULTABA SER UNA MOLÉCULA COVALENTE APOLAR.
GRACIAS.
Black Dragon -
muy bien