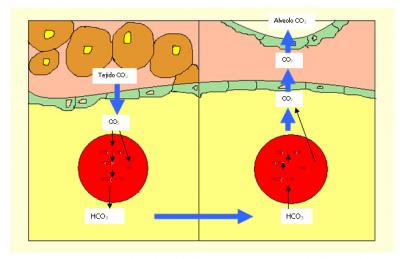
En todo momento, nuestro cuerpo está consumiendo oxígeno a razón de unos 240 ml por minuto en actividad normal. Las distintas partes del organismo necesitan el O2 para, por reacción con los hidratos de carbono, producir energía. Es la sangre quien se encarga de transportarlo de los pulmones a las células, y, como sabemos, es este proceso se libera CO2.
Las reacciones de intercambio gaseoso de la sangre en los pulmones, (alvéolos), y en los tejidos dependen básicamente de la afinidad* del O2 y del CO2 por la hemoglobina y la mioglobina, así como de las presiones parciales de estos gases a nivel de alvéolos y tejidos.
*Entendemos como afinidad la capacidad de reacción de estas sustancias con el O2 y el CO2. En el caso de la hemoglobina, su afinidad es mayor para el CO2 que para el O2. Por su parte, la mioglobina tiene mayor afinidad por el O2 que la hemoglobina.
*Una molécula de hemoglobina es una estructura compleja formada por cuatro cadenas de proteína, cada una de las cuales se enlaza con un grupo molecular en forma de anillo, el grupo hemo, que contiene un ión Fe+2 en su centro. Por su parte, la mioglobina está formada por una sola cadena proteínica unida a un grupo hemo con un Fe+2 en su centro. Las presiones parciales del O2 y del CO2, (en mm de Hg), son:
| | GASES | ALVÉOLO | TEJIDOS |
| | O2 | 100 | 40 |
| | CO2 | 40 | 42-46 |
La sangre contiene glóbulos rojos y en cada uno de ellos hay varios cientos de millones de moléculas de hemoglobina. Son ellas las encargadas del transporte del oxígeno.
Por tanto, según lo anteriormente mencionado, las reacciones serán:
ü En cuanto al oxígeno, (O2):
(El oxígeno se liga al hierro de la hemoglobina).
Hb + O2 à HbO2- (oxihemoglobina)
Como podemos observar en el cuadro de las presiones parciales anterior, el oxígeno saldrá de los alvéolos hacia los tejidos, ya que la presión parcial de este gas en el interior del alvéolo es mayor que la existente en los tejidos.
Así pues, en los pulmones, donde la concentración de O2 es elevada, la reacción se desplaza casi totalmente a la derecha formándose oxihemoglobina.
El curso de la reacción hacia la derecha está favorecido por algunos factores:
a) altas tensiones de O
2 b) temperatura discretamente baja
c) tendencia hacia la alcalinidad
Estas condiciones reinan a nivel del pulmón; por esto, Hb pasa a HbO2. A nivel de los tejidos, como veremos a continuación, predomina el proceso opuesto.
- A nivel de tejidos el O2:
Después de la formación de oxihemoglobina, la sangre prosigue su circulación a través de arterias y capilares y llega a los tejidos. Allí, donde la concentración de CO2 es pequeña, se produce un desplazamiento del equilibrio hacia la izquierda. La sangre pierde alrededor del 45% del oxígeno que transportaba.
HbO2- à Hb + O2 Por tanto, ante lo anteriormente expuesto, podríamos establecer el siguiente equilibrio químico.
Hb + O2 ⇄ HbO2- El oxígeno es recogido por las células y almacenado en ella gracias a la mioglobina, (Mb). Por lo que, podemos igualmente escribir:
O2 + Mb à MbO2 ü Con respecto al dióxido de carbono, (CO2):
La hemoglobina, tras descargarse de O2 en los capilares, puede transportar hasta los pulmones el CO2 producido en los procesos de oxidación de las células. El enlace de la hemoglobina con el CO2 no tiene lugar por el grupo hemo, sino por un extremo de las cadenas proteínicas.
A nivel de tejidos el CO2:
(El dióxido de carbono no se liga al hierro, sino al grupo amino de la hemoglobina).
HbNH2+ CO2 à HbNHCOOH
Como podemos observar en el cuadro de las presiones parciales anterior, el dióxido de carbono posee una presión parcial mayor en los tejidos que en los alvéolos pulmonares.
- A nivel de alvéolos el CO2:
Es el proceso opuesto al anterior.
HbNHCOOH à HbNH2+ CO2
Por tanto, ante lo anteriormente expuesto, podríamos establecer el siguiente equilibrio químico:
HbNH2+ CO2 à HbNHCOOH
Además, la hemoglobina puede también unirse con iones H+, con lo que teniendo en cuenta el equilibrio que existe en la sangre:
CO2 + H2O ⇄ HCO3- + H+ (aq) Permite disolver más CO
2, facilitando su separación de los tejidos. En los pulmones el proceso se invierte y el CO
2 deja la disolución y es exhalado. Para hacernos una idea, el aire inhalado contiene un 20% de O
2 y un 0,04% de CO
2, y el exhalado, un 16% de O
2 y un 4% de CO
2. Hay moléculas similares en estructura al O2, como NO, (e incluso el ión CN-), pero con mayor afinidad por la hemoglobina, por lo que pueden desplazar al O2 de ésta:
HbO2 + CO ⇄ HbCO + O2
Este equilibrio está muy desplazado hacia la derecha. Ésta es la causa de que el CO, producido en las combustiones incompletas, (escape de automóviles, etc.), sea un gas venenoso.
Por el mismo motivo, entre los fumadores no es raro encontrar individuos con más de un 20% de la hemoglobina bloqueada por el CO del humo del cigarrillo.