Reacciones de combustión
DEFINICIÓN.
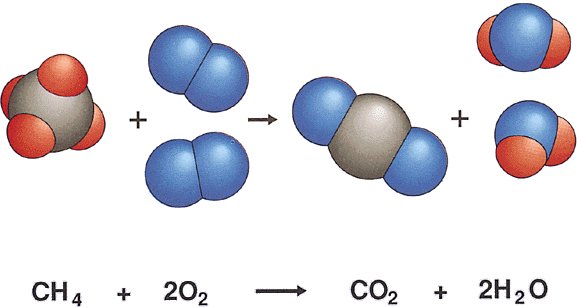
La reacción de combustión se basa en la reacción química exotérmica de una sustancia o mezcla de sustancias llamada combustible con el oxígeno. Es característica de esta reacción la formación de una llama, que es la masa gaseosa incandescente que emite luz y calor, que esta en contacto con la sustancia combustible.
La reacción de combustión puede llevarse a cabo directamente con el oxígeno o bien con una mezcla de sustancias que contengan oxígeno, llamada comburente, siendo el aire atmosférico el comburente mas habitual.
CALOR DE REACCIÓN.
El calor de reacción, Qr se define como la energía absorbida por un sistema cuando los productos de una reacción se llevan a la misma temperatura de los reactivos, también es necesario especificar la presión. Si se toma la misma presión para ambos, el calor de reacción es igual al cambio de entalpía del sistema, DH r.
Los calores de formación se calculan experimentalmente, pero puede ocurrir que en la práctica no podamos llevar a cabo la formación de un producto. En estos casos se hace uso de los calores de combustión.
Ejemplo: C + 2S > CS2
Una manera de producir calor es mediante una reacción química de combustión.
En las reacciones de combustión obtenemos calor combinando un combustible (gasolina, butano, madera...) con el oxígeno del aire.
El calor generado al transformarse el combustible vaporiza los componentes originados y hace saltar sus electrones a niveles más altos. Al desexcitarse emiten luz y calor.
El tipo de luz que emiten depende de los componentes gaseosos excitados.
En las combustiones de compuestos que contienen carbono siempre se producen CO2 y H2O con algo de CO.
La forma de la llama nos indica si la combustión es rica o pobre.
En los estudios sobre las zonas de la llama se especifican estas partes:

1.- Cono frío: no llega oxígeno
2.- Cono de reducción: poco oxígeno
3.- Cono de oxidación: abundancia de oxígeno
4.- Zona de fusión: alcanza los1500 ºC
IMPLICACIONES SOCIALES Y AMBIENTALES.
Las reacciones de combustión provocan problemas medioambientales como el agotamiento de los recursos fósiles, contaminación y aumento del efecto invernadero.
La importancia que tienen los procesos químicos que conllevan una reacción química es que sin ellos no podría existir la vida humana ya que en varios procesos se crea el dióxido de carbono el cual lo inhalamos y al exhalarlo se convierte en CO2 y esto también demuestra que el ser humano dentro de sus funciones tiene procesos químicos.
También estas mismas reacciones químicas tienen una gran importancia socioeconómica ya que con estas hemos logrado un gran avance tecnológico y socioeconómico pues se ha logrado a base de buenas investigaciones y procesos químicos.
Gracias al gran manejo de investigación y desarrollo sobre las reacciones químicas se han podido hacer varios avances científicos, los cuales se basan en las satisfacciones y comodidades del hombre; también gracias a estas investigaciones podemos entender mejor los procesos químicos, causas y consecuencias de estos mismos.
5 comentarios
yany -
yany -
juan -
ivan -
jose vivanco -